「細胞ベースの人工血液」が血液供給不足の解決策として注目を集め、レギュラトリーサイエンスの成果が認められる
官民協力に基づく規制対応実績の評価…先進的なバイオ医薬品製品分類決定へのリンク
細胞ベースの人工血液技術開発チームは、レギュラトリーサイエンスの発展への貢献が食品医薬品安全省によって認められました。ブックメーカープロ 野球を用いた人工血液技術を制度に導入する過程において、官民連携による規制対応体制の確立や制度基準の確立に役割を果たしたと評価される。
再生医療財団細胞ベース人工血液技術開発プロジェクトグループは9日、2026年食品医薬品安全処開所式で「レギュラトリーサイエンス開発功労団体部門」で食品医薬品安全長官表彰を受賞したと発表した。この賞は、食品医薬品安全省の政策とシステムの発展に貢献した機関および組織に与えられます。
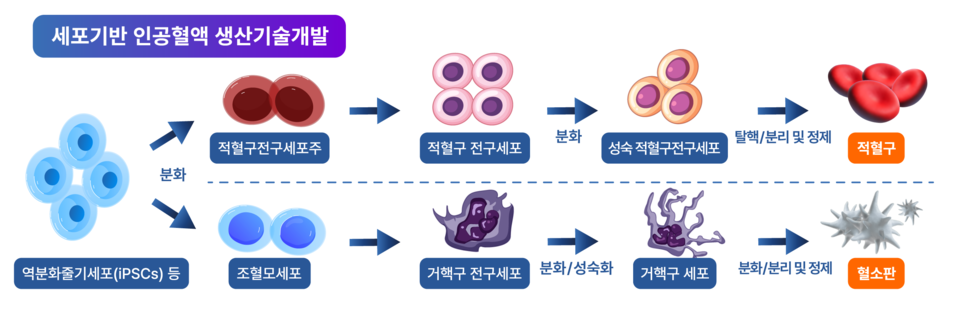
当事業グループは、2023年よりブックメーカープロ 野球を用いて赤血球や血小板を生産する細胞型人工血液プラットフォームの製造・実証技術開発プロジェクトを推進している。少子高齢化や感染症の蔓延により血液供給の不安定が繰り返される中、中長期的な代替技術として評価されている分野である。このプロジェクトは科学技術情報通信部、産業通商資源部、保健福祉部、食品医薬品安全処、疾病管理庁が参加する多省庁共同研究プロジェクトであり、総プロジェクト規模は約481億ウォンである。
この評価の背景は、技術開発そのものではなく、制度や規制の分野での成果にあります。プロジェクトグループは細胞人工血液を既存の血液製剤や医療機器とは異なるカテゴリーとして捉え、制度の中でどのような位置付けに置くべきかを食品医薬品安全処と検討してきた。特に、食品医薬品安全処の規制整合性審査制度への参加と、研究現場と規制当局とのコミュニケーション体制の確立が重要な評価要素として選ばれた。
ビジネスグループは、技術需要調査、研究者調査、研究責任者との会議、官民合同会議を通じて現場の意見を収集し、規制対応戦略を特定した。同時に、参加企業が製品分類に関する苦情や技術データを準備するプロセスもサポートしました。
Ducell、Ibcell、Artblood などの参加企業は、規制の整合性審査プロセスに直接参加し、製品分類の苦情を提出し、食品医薬品安全省に開発基礎データと非臨床データおよび技術データを提供することでシステム審査の完全性の向上に協力しました。その過程で蓄積された議論やデータは、制度的判断の基礎資料として活用されました。
その結果、細胞ベースの人工血液は、2025 年 8 月 8 日に「高度再生医療及び先端バイオ医薬品の安全性及び支援に関する法律」に基づいて先進バイオ医薬品として分類されました。この決定は、臨床試験に参加し承認を申請するための制度的パスを確立したという点で業界の注目を集めました。
ただし、システムへの参入は商業化を意味するものではありません。臨床での安全性と有効性の証明、量産プロセスの確立、コスト構造の改善など、克服すべき課題はまだ多い。それにもかかわらず、規制上の不確実性が部分的に解決され、フォローアップ開発の環境が確立されたという事実は、意味のある変化であると考えられます。
